Aufgabe 12
Aufgabe I:
1 Leitet man Wasserdampf über stark erhitzten Koks
(Kohlenstoff), entsteht ein Gasgemisch, das in der
chemischen Industrie in vielfältiger Weise verwendet wird.
In einer ersten Gleichgewichtsreaktion (A) entsteht ein
Gemisch aus Kohlenstoffmonooxid und Wasserstoff. In einer
zweiten Gleichgewichtsreaktion (B) reagiert das
Kohlenstoffmonooxid mit Wasserdampf exotherm zu
Kohlenstoffdioxid und Wasserstoff.
1.1 Formulieren Sie
für beide Reaktionen jeweils eine Reaktionsgleichung.
1.2
Geben Sie am Beispiel des Gleichgewichts (B) Möglichkeiten
an, die Ausbeute der Produkte zu erhöhen, und begründen Sie
Ihre Aussagen.
2 Bei einer Ausgangskonzentration der Edukte von jeweils
c = 0,1 mol * l–1
wird im Gleichgewicht (B) eine Konzentration c(CO2)
= 0,05 mol * l–1
erreicht.
2.1 Geben Sie für das Gleichgewicht (B) das
Massenwirkungsgesetz an und berechnen Sie den Wert der
Gleichgewichtskonstanten.
2.2 Berechnen Sie die
Konzentration aller beteiligten Stoffe im Gleichgewicht für
den Fall, dass die Ausgangskonzentration von Wasserdampf
verdoppelt und die von Kohlenstoffmonooxid mit c = 0,1 mol *
l–1 beibehalten
wird.
3 Kohlenstoffdioxid kann durch Auswaschen mit Kalkwasser
(gesättigte Lösung von Calciumhydroxid) aus dem
Gleichgewicht entfernt werden.
Beschreiben Sie, was dabei
beobachtet werden kann und erläutern Sie dies anhand einer
Reaktionsgleichung.
4 Berechnen Sie für Normalbedingungen das Volumen der Stoffportion Wasserstoff, die entsteht, wenn eine Tonne Koks vollständig zu Kohlen-stoffdioxid umgesetzt wird.
5 Aus Kohlenstoffmonooxid und Wasserstoff können unter
verschiedenen Reaktionsbedingungen Methan, Methanol oder
Essigsäure (Ethansäure) synthetisiert werden.
Formulieren
Sie jeweils eine Reaktionsgleichung.
Aufgabe II:
1 Honig enthält u. a. das Trisaccharid Melezitose.
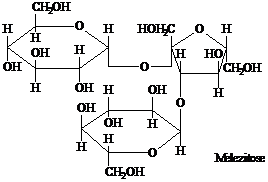
1.1 Benennen Sie die Monosaccharidbausteine und erläutern
Sie den Aufbau des Trisaccharids.
1.2 Beschreiben Sie
einen experimentellen Weg, wie dieses Trisaccharid
hydrolysiert werden kann.
Benennen Sie eines der beiden
bei der Hydrolyse entstehenden Disaccharidmoleküle mit dem
Trivialnamen.
Begründen Sie das Verhalten der beiden
Disaccharide bei der Fehling-Probe.
1.3 Das Monosaccharid
Fructose reagiert mit Fehling‘scher Lösung, da es in
alkalischem Milieu mit den beiden Aldosen Glucose und
Mannose im Gleichgewicht steht.
Zeichnen Sie die
Strukturformeln dieser Aldosen in der Fischer-Projektion.
Erklären Sie die Tatsache, dass zwei Aldosen entstehen.
Zeichnen Sie die Strukturformel des Produkts, das durch
Oxidation am Kohlenstoffatom C-1 des Mannosemoleküls
entsteht.
1.4 In saurer Lösung liegen Fructosemoleküle
auch in zwei Pyranoseformen (= Sechsringe) vor.
Zeichnen
Sie deren Strukturformeln in der Haworth-Projektion und
benennen Sie diese.
2 Kohlenhydrate werden im Körper nahezu vollständig zu
Kohlenstoffdioxid und Wasser umgesetzt. Der für den Nährwert
maßgebliche physiologische Brennwert ist fast genauso groß
wie der im Verbrennungskalorimeter messbare physikalische
Brennwert.
Berechnen Sie mit Hilfe der angeführten
Tabellenwerte den Brennwert von 100 g Saccharose.
| Saccharose (s) | Kohlenstoffdioxid (g) | Wasser (l) | |
| ΔHf0 in kJ * mol-1 | -2222 | -393 | -286 |
Aufgabe III:
1 Formulieren Sie für die Bildung von Polyethin aus den Monomeren eine Reaktionsgleichung unter Verwendung von Strukturformeln.
2.1 Erklären Sie mit Hilfe des Orbitalmodells die
Bindungsverhältnisse und die räumliche Anordnung der Atome
im Polyethinmolekül.
Leiten Sie daraus eine Erklärung für
die elektrische Leitfähigkeit ab.
2.2 Durch Verstrecken
des Kunststoffs wird seine elektrische Leitfähigkeit
verbessert.
Geben Sie dafür eine mögliche Erklärung.
3 Beschreiben Sie mit Hilfe des Elektronengasmodells die
Bindungsverhältnisse bei Metallen.
Erklären Sie die gute
Verformbarkeit und die elektrische Leitfähigkeit der
Metalle.
4 Polyethin kann mit Styrol zur Reaktion gebracht werden,
wobei ein Kunststoff mit neuen Eigenschaften entsteht.
4.1 Formulieren und erläutern Sie den zugrunde liegenden
Reaktionsmechanismus.
4.2 Zeichnen Sie einen sinnvollen
Formelausschnitt aus dem entstandenen Makromolekül.
4.3
Erklären Sie die Unterschiede zwischen Polyethin und dem neu
entstandenen Kunststoff bezüglich ihrer thermischen
Eigenschaften und ihrer elektrischen Leitfähigkeit.
Aufgabe IV:
Ein wichtiges Zinkerz ist die Zinkblende (Zinksulfid,
ZnS), die häufig als Beimengungen Blei- und Sibersulfid
enthält.
Zur Zinkgewinnung wird das Erz zunächst
geröstet. Man erhält verunreinigtes Zinkoxid, das nach zwei
verschiedenen Verfahren (A) und (B) zu Zink umgesetzt werden
kann.
1 Beim Röstprozess wird bei hohen Temperaturen Luft
über Zinksulfid geleitet. Dabei entstehen Schwefeldioxid und
Zinkoxid.
Formulieren Sie hierzu eine Reaktionsgleichung
mit Oxidationszahlen.
2 Beim trockenen Verfahren (A) wird Zinkoxid mit
Kohlenstoff bei hohen Temperaturen zur Reaktion gebracht.
Dabei entstehen Kohlenstoffmonooxid und flüssiges Rohzink.
Stellen Sie die Reaktionsgleichung für die Reduktion von
Zinkoxid auf.
Zur Reinigung wird das Zink abdestilliert.
Geben Sie an, worauf dieses Reinigungsverfahren beruht.
3 Beim nassen Verfahren (B) wird das Röstprodukt mit
Schwefelsäure umgesetzt. Die entstehende Lösung wird zur
Reinigung mit Zinkpulver versetzt und das Zink anschließend
elektrolytisch abgeschieden.
3.1 Stellen Sie für die
Reaktion zwischen Zinkoxid und Schwefelsäure die
Reaktionsgleichung auf und benennen Sie den Reaktionstyp.
3.2 Erläutern Sie mit Hilfe einer Reaktionsgleichung die
Wirkungsweise des zugegebenen Zinkpulvers und begründen Sie
die Notwendigkeit dieses vorgeschalteten
Reinigungsverfahrens.
3.3 Formulieren Sie die
Reaktionsgleichungen für die denkbaren Kathodenreaktionen
und berechnen Sie die Elektrodenpotentiale. Gehen Sie dabei
von einer Zinkionen-Konzentration c = 1 mol * l–1
und einem pH = 5 aus. Vergleichen Sie das Ergebnis der
Rechnung mit dem experimentellen Befund.
4 Obwohl Zink ein unedles Metall ist, wird es als
Überzugsmetall für Eisenbleche verwendet, um diese vor
Korrosion zu schützen.
4.1 Erklären Sie, worauf die
Schutzwirkung des unbeschädigten Zinküberzugs beruht.
Erläutern Sie mit Hilfe einer beschrifteten Skizze, welche
Vorgänge bei der Beschädigung des Überzugs bei Einwirkung
saurer Lösungen ablaufen.
4.2 Bettet man einen mit
Zinkdraht verbundenen Eisennagel in mit neutraler, wässriger
Phenolphthalein-Lösung versetzte Gelatine ein, so verfärbt
sich der Bereich um den Eisennagel rotviolett.
Erklären
Sie dieses Versuchsergebnis und formulieren Sie die
Reaktionsgleichungen
Lösung(BW20)
