
Hybridorbitale
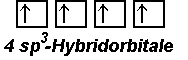
Die durch die Berechnung der Aufenthaltswahrscheinlichkeit der jeweiligen von den Elektronen erzeugten Orbitale stimmen nicht immer mit den aufgrund chemischer Eigenschaften zu vermutenden Formen überein. So stellt man fest, dass das Kohlenstoffatom in der äußeren Elektronenschale zwei s- und zwei p-Elektronen besitzt. Dementsprechend müssten diese Orbitale bei den C-H-Bindungen im Methan (CH4) zu unterschiedlichen Bindungen führen. Tatsächlich stellt man aber fest, dass die vier Bindungen gleichartig und nicht unterscheidbar sind. Dies kann man durch sp3-Hybridisierung erklären: Das doppelt besetzte, kugelförmige 2s-Orbital wird mit den hantelförmigen 2p-Orbitalen (2 einfach besetzt, eins unbesetzt) zu vier gleichen, keulenförmigen sp3-Hybridorbitalen kombiniert, die mit je einem Elektron besetzt sind. Diese richten sich tetraedrisch im Raum aus und bilden mit den 1s-Elektronen des Wasserstoffs gleichartige Atombindungen. Das so entstandene Modell entspricht den beobachteten Eigenschaften des Methans.
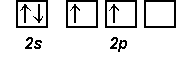
Carbeniumionen bzw. Kohlenstoffatome in Doppelbindungen sind
grundsätzlich sp2-hybridisiert,
in Dreifachbindungen sind sie sp-hybridisiert.